
Colocar sal no gelo dentro de um isopor faz a bebida gelar mais rápido?
O físico Wil Namen ensina que é possível reduzir o tempo para gelar uma bebida usando apenas três ingredientes que estão em qualquer cozinha: água, gelo e sal.
Vamos entender o porquê desse fenômeno?
Para a ciência, resfriar significa perder calor. A adição do sal diminui a temperatura de fusão (temperatura na qual uma substância passa do estado sólido para o líquido) do gelo. Portanto, ele passa a derreter bem mais rápido já que a água líquida conduz melhor o calor do que o gelo, e, para isso, usa energia do ambiente (e da latinha também). Perdendo energia, que é o mesmo que calor, a temperatura da lata diminui. Com isso o líquido resultante da mistura de gelo e sal está a uma temperatura abaixo de 0°C.
Tudo isso faz com que a energia térmica da bebida seja removida com maior velocidade, tornando a bebida mais gelada em menos tempo!

Quimicamente falando, ao adicionar sal ao gelo, ocorre forte interação entre as moléculas dessas duas substâncias, dificultando a organização dos cristais de gelo e diminuindo a temperatura, solidificando. Essa propriedade é denominada de Crioscopia.

Para que uma substância passe do estado líquido para o sólido, as suas moléculas precisam perder energia cinética. Existem alguns fatores que influenciam nessa transição, entre eles está o tipo de forças intermoleculares de cada substância. Quanto menores ou mais fracas forem as forças de atração das moléculas, menor será o ponto de congelamento. Assim, o ponto de solidificação (temperatura na qual uma substância passa do estado líquido para o sólido) da água é 0°C ao nível do mar. No entanto, ao adicionar o sal, esse é fortemente atraído pelas moléculas de água, dificultando a organização dos cristais de gelo e, consequentemente, diminuindo seu ponto de congelamento. Comparando numa solução com 10% de sal, o ponto de congelamento cairá para -6°C e com 20%, para -16°C, ou seja, em 5 minutos seu isopor será capaz de fazer por sua latinha de cerveja o que o freezer faria em 15 minutos. Se você tem pressa, triture as pedras. Quanto maior for a superfície de contato da mistura com as latinhas, mais rápido é o resfriamento.
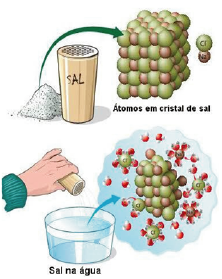
Somente a adição de sal funciona para que a bebida fique gelada mais rápido.
Mito: podemos utilizar outras substâncias.
A experiência também funciona com o açúcar ou qualquer outra substância que seja solúvel em água e não seja volátil. Isso porque o composto adicionado impede que as moléculas de água se organizem para formar a estrutura sólida. Desse modo, experimentalmente podemos comprovar que a adição de um soluto não volátil a um solvente dá origem a uma solução que tem o ponto de solidificação menor que o solvente puro.
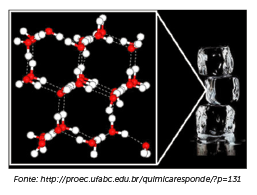
Curiosidades!
Você sabia que devido a essa propriedade da crioscopia, em países onde costuma nevar, coloca-se sal nas ruas para ajudar no derretimento do gelo? Com isso as estradas e rodovias são liberadas mais rapidamente para circulação de veículos.
Apesar das vantagens da adição de sal, com o derretimento da neve, há a formação de uma película de água líquida sobre as rodovias, o que ocasiona na diminuição do atrito entre os pneus e o solo, aumentando o risco de ocorrência de derrapagens. Portanto, adiciona-se areia juntamente ao sal sobre a neve. A areia auxilia de forma a aumentar a aderência dos pneus ao solo, diminuindo assim o risco de acidentes.
Outro fato muito curioso é que a Crioscopia também explica o porquê de os oceanos não se congelarem completamente, mesmo em regiões nas quais a temperatura ambiente é abaixo de zero grau Celsius. A água do mar possui sais dissolvidos nela, que dificultam a organização das moléculas de água e consequente solidificação.

 Congregação de São João Batista
Congregação de São João Batista



